Phân biệt các hợp chất là một chủ đề quan trọng dành cho những giáo viên và học sinh quan tâm. Tôi hy vọng tài liệu này sẽ hữu ích trong việc nghiên cứu và tìm hiểu thêm về chủ đề này.
1. Lý thuyết
a. Với chất khí.
b. Dung dịch bazơ.
Chất lỏng có tính axit.
d. Dung dịch muối.
e. Các oxit của kim loại
Thông thường hòa tan vào nước-> được phân thành hai nhóm: Tan trong nước và không tan trong nước.
Các nhóm thuộc nội địa có tác dụng với khí CO2 (nếu thử bằng giấy quỳ tím sẽ chuyển sang màu đỏ).
Trường hợp không xuất hiện kết tủa: Kim loại tring oxit được xem là kim loại kiềm (Hóa trị I).
Nếu xuất hiện kết tủa, các kim loại trong oxit thuộc nhóm kim loại kiềm thổ (Hóa trị II).
Nhóm không tan trong nước có hiệu quả khi tác dụng với dung dịch kiềm (NaOH).
Khi đưa vào dung dịch kiềm, các kim loại trong oxit bao gồm Al, Zn, Cr.
Nếu không tan trong chất kiềm, thì đó là một kim loại khác.
Những hợp chất oxit phi kim: Khi thử đưa vào nước bằng quỳ tím -> Chuyển sang màu xanh.

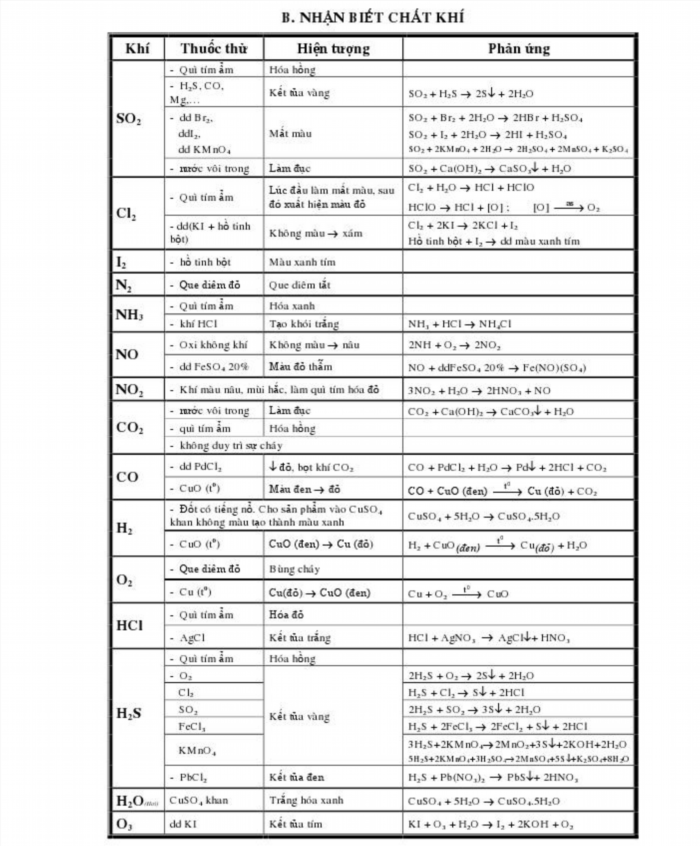
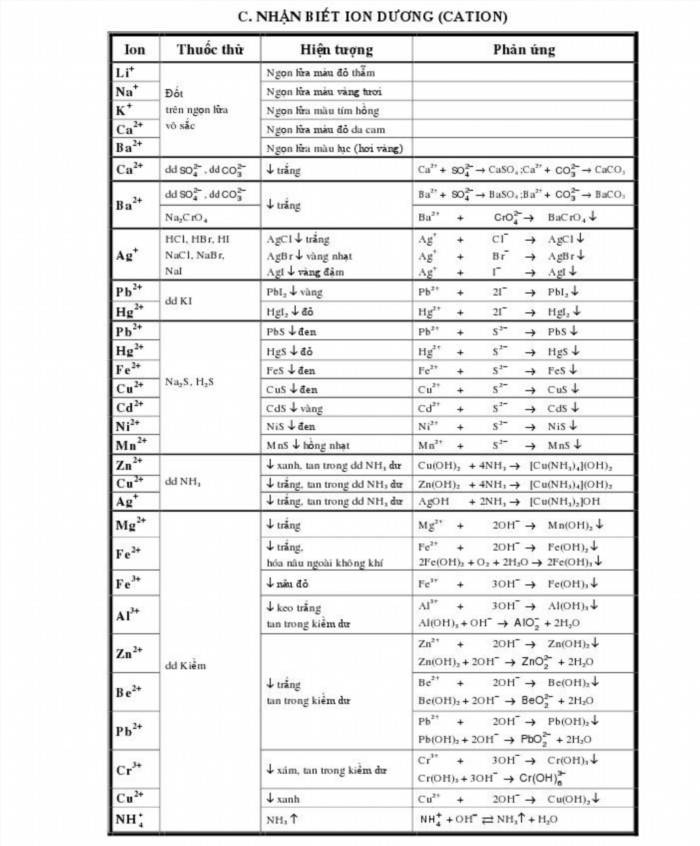

Chủ đề phân biệt các hợp chất.
2. Bài tập
Vấn đề thứ nhất: Phân biệt các hợp chất dựa trên tính chất vật lý.
Dạng bài tập này có thể dựa trên các đặc tính vật lý khác nhau như: sắc thái, hương vị, tính tan.
Không phát sinh CO2, sắt bị hút bởi nam châm, Khí NH3 có mùi hăng, khí H2S có mùi hôi trứng, đều là những đặc điểm đặc trưng của các chất.
Dựa vào thuộc tính vật lý, hãy phân biệt giữa hai loại bột AgCl và AgNO3.
BL: + Lấy một ít mẫu từng chất để thử.
Thêm vào nước hai mẫu thử, chất bột AgNO3 hoà tan trong nước còn AgCl thì không tan được.
Nhận biết các loại bột như AgNO3, Fe và Cu dựa trên tính chất vật lý của chúng.
Nhận biết ba loại khí Cl2, O2, CO2 dựa trên tính chất vật lý riêng của chúng.
Dựa vào tính chất vật lý, hãy phân biệt các chất trong lọ không có nhãn.
Chủ đề phân biệt các hợp chất.
Vấn đề thứ hai: Phát hiện các hợp chất dựa trên đặc tính hóa học.
Kiểu 1: Nhận ra bằng cách sử dụng thuốc thử tùy chọn.
Thông thường, chúng ta hòa tan các chất rắn vào nước và sau đó xác định sản phẩm thu được.
Bằng phương pháp hoá học, hãy phân biệt các loại chất rắn sau đây:
A) Canxi oxide and Sodium oxide b) Calcium oxide and Calcium carbonate c) Calcium oxide and Magnesium oxide d) Calcium oxide and Phosphorus pentoxide.
E) Nhôm và sắt. F) Nhôm, sắt và bạc. G) Muối natri clorua (NaCl), nitrat natri (NaNO3), carbonate bari (BaCO3), và sulfat bari (BaSO4). H) Carbonate natri (Na2CO3), carbonate magiê (MgCO3), và carbonate bari (BaCO3).
Sử dụng kỹ thuật hoá học để phân biệt các loại bột trắng sau đây:
B) Xoài, dừa, đu đủ. A) Tinh bột, cellulose, sucrose. B) Mango, coconut, papaya.
B) Tinh bột, đường glucose và đường mía.
Thông thường, chúng ta sử dụng các khí này để thử nghiệm và xác định.
Bằng cách sử dụng phương pháp hóa học, hãy nhận diện các loại khí sau đây:
A) Khí CO2 và O2 b) Khí SO2 và O2 c) Khí CO2 và SO2.
D) Clorua, axit clohidric, ôxy. E) Cacbon dioxit, clorua, cacbon monoxit, hidro. F) Cacbon dioxit, khí sunfur dioxide, ôxy, amoniac, ethin, etylen.
Xác định các chất khí sau đây bằng cách sử dụng phương pháp hóa học:
A) Khí carbon dioxide, methane và acetylene. B) Khí methane và ethylene. C) Khí methane, ethylene và acetylene. D) Khí methane, carbon dioxide, acetylene và oxygen.
Thường dùng những chất này để thử nghiệm trong thuốc.
Đề xuất phương pháp hóa học để phân biệt các dung dịch sau đây:
A) Acid HCl và H2SO4 b) Acid HCl, H2SO4, HNO3. C) Acid HCl, H2SO4, HNO3, khí H2.
D) HCl, H2SO4, HNO3, và H3PO4. E) HCl, H2SO4, HNO3, H3PO4, cùng với H2O.
Phân biệt các chất lỏng sau đây bằng kỹ thuật hóa học:
A) Natri clorua (NaCl) và natri sunfat (Na2SO4).B) Đa số các hợp chất hòa tan trong nước đều có khả năng tạo ra dung dịch dẫn điện.
B) Muối biển, muối sunfat natri, nitrat natri.
C) Natri sulfat và Đồng sulfat.
D) Natri sunfat, đồng sunfat và muối Natri clorua.
E) Muối đồng sulfate, nitrat bạc và muối natri clorua.
F) K2SO4 và Fe2(SO4)3.
G) K2SO4, FeSO4, và Fe2(SO4)3.
H) MgSO4, Na2SO4, FeSO4, và CuSO4.
I) FeSO4, Fe2(SO4)3 và MgSO4 được sử dụng trong các phương pháp xử lý nước. Ii) Hỗn hợp của FeSO4 và MgSO4 được áp dụng trong các kỹ thuật xử lý nước.
Đề xuất cách phân loại các chất lỏng dựa trên phương pháp hóa học.
A) Na2SO4 và axit sunfuric.B) Xin hãy cho thêm 10ml dung dịch NaOH vào dung dịch HCl. A) Na2SO4 và axit sulfuric.
B) Sodium sulfate, sulfuric acid, and sodium chloride.
C) Muối ăn, muối sulfat natri và axit sulfat.
D) Muối biển, axit clohidric, axit sulfuric.
E) Na2SO4, axit sunfuric, axit clohidric.
F) Na2SO4, NaCl, H2SO4 và HCl.
Hãy nhận ra những ống nghiệm không có nhãn chứa các dung dịch sau đây:
A) Na2CO3, NaOH, NaCl và HCl. B) Nước là một phân tử không có tính chất điện tích.
B) HCl, NaOH, Na2SO4, NaCl, và NaNO3.
Những hợp chất NaNO3, Mg(NO3)2, Fe(NO3)2, Cu(NO3)2.
D) Natri cacbonat, Amoni nitrat, Axit clohidric, Sắt(II) clorua.
E) Muối NaCl, NaNO3, Na2SO4, Na2S, Na2CO3, Na2SO3.
F) FeSO4; Fe2(SO4)3 và MgSO4.
Hãy đề xuất phương pháp hóa học để phân biệt giữa 2 dung dịch Glucozơ và rượu etylic.
Có 2 lọ không có nhãn chứa 2 dung dịch vô màu: axit axetic và etanol. Hãy miêu tả.
Sử dụng phương pháp hóa học để phân biệt giữa rượu etylic và axit axetic từ ba chất lỏng bao gồm rượu etylic, axit axetic và dầu ăn hòa tan trong rượu.
Phân biệt 2 chất lỏng trên bằng phương pháp hóa học là: Rượu tylic, axit axetic và glucozơ là 3 chất lỏng.
Đưa ra công thức phản ứng và giải thích cách phân biệt các chất lỏng được lưu trữ trong từng lọ riêng biệt bao gồm CH3COOH, C6H6, C2H5OH và C6H12O6 dựa trên phương pháp hóa học.
Chủ đề phân biệt các hợp chất.
Phương pháp nhận diện bằng cách sử dụng thuốc thử theo quy định.
Trường hợp này không áp dụng nhiều loại dược kiểm tra mà chỉ thực hiện dược kiểm tra theo quy định của đề bài.
Chúng ta sử dụng chất thử để xác định lọ chứa chất thử cho các lọ còn lại. Do đó, lọ được phát hiện là một trong những lọ đã được cung cấp.
Chỉ sử dụng quỳ tím, hãy phân biệt các ống nghiệm không có nhãn chứa các chất lỏng sau đây:.
Acid sunfuric, muối natri sunfat và cloa bari.
B) H2SO4, Na2SO4, BaCl2, và NaCl.
C) Natri hydroxit, axit clohidric, nước d) Axit clohidric, axit sunfuric, barium clorua.
E) Na2SO4, axit sulfuric, NaOH f) Na2SO4, Na2CO3, axit sulfuric, BaCl2.
G) Muối ăn, axit sulfuric, kali hydroxit h) Axit clohidric, muối ăn, natri carbonat, clo bari.
Chỉ sử dụng màu tím, hãy phân biệt các dung dịch bằng cách đặt từng lọ riêng biệt trên một tấm tròn.
A) Các chất như Sodium hydroxide, silver nitrate, hydrochloric acid, nitric acid, hydrogen phải được sử dụng trong phòng thí nghiệm với đầy đủ các quy định an toàn và trang thiết bị bảo hộ. B) Để đảm bảo an toàn trong phòng thí nghiệm, chúng ta cần phải đeo đầy đủ trang thiết bị bảo hộ và tuân thủ các quy định an toàn.
B) Na2CO3, NaOH, HCl và Ba(OH)2.
C) H2SO4, NaOH, BaCl2, và (NH4)2SO4.
D) Clouađi clorua, hidroxit natri, muối natri, clouađi nhôm.
E) Na2SO4, Na2CO3, NaCl, H2SO4, BaCl2 và NaOH.
F) HCl, Na2CO3, AgNO3 và BaCl2.
G) NaHSO4, Na2CO3, Na2SO3, BaCl2 và Na2S.
H)BaCl2,NH4Cl;(NH4)SO4;NaOH;Na2CO3.
Chỉ được sử dụng thêm một loại thuốc thử khác, xin hãy phân biệt các hợp chất sau đây:
Trong thí nghiệm đó, chúng ta sử dụng Na2CO3 để tạo ra khí CO2, sau đó thổi khí CO2 vào dung dịch HCl để thu được muối NaCl và nước. Cuối cùng, chúng ta thêm dung dịch Ba(NO3)2 vào dung dịch đã có muối NaCl để kiểm tra sự hiện diện của ion Cl- trong dung dịch.
B) Natri sunfat, natri cacbonat, axit sulfuric, bari clorua.
C) Muối natri cacbonat, axit clohidric, muối bari nitrat, muối natri sunfat.
D) Ba(OH)2, NH4Cl, HCl, và (NH4)2SO4.
E) FeCl2, FeCl3, NaOH, và HCl.
F) Natri cacbonat, Bari clorua, Acid sulfuric.
H2SO4, Ba(NO3)2, KCl, Na2 là các hợp chất hóa học.
H) Acid clohidric, Bazơ natri, Nitrat bạc và Sulphat đồng là những chất hóa học được liệt kê.
I) Muối MgCl2, FeCl2, FeCl3, AlCl3.
J) H2SO4, Na2SO4, Na2CO3 và MgSO4.
K) Acid clohidric, axit sulfuric và bari clorua.
L) NH4HSO4, Ba(OH)2, BaCl2, HCl, NaCl và H2SO4 là các chất hóa học được đề cập.
Chỉ sử dụng dung dịch HCl để phân biệt các chất sau đây:
A) Muối NaCl, Na2CO3, BaSO4 và BaCO3 đều có thể tan trong nước.Hợp chất này có khả năng hòa tan trong dung dịch nước giống như các muối NaCl, Na2CO3, BaSO4 và BaCO3.
B) Sắt, oxit sắt, đồng.
C) Đồng, đồng oxit, kẽm.
D) Muối, soda lạnh, muối magie và xút natri.
Sử dụng chỉ dung dịch brom để phân biệt các khí sau đây:
B) Hợp chất hữu cơ như chất axit amin và este. A) Các phân tử methane (CH4) và ethylene (C2H4). B) Các hợp chất hữu cơ như chất axit amin và este.
B) Các chất khí CH4 và C2H2.
C) Các hợp chất C2H4 và C2H2.
D) Carbon dioxide, ethylene, acetylene.
Sử dụng chỉ dung dịch NaOH để phân biệt giữa các dung dịch.
B) Tất cả các chất trên đều là muối. A) Natri clorua, amoni clorua, magie clorua, sắt(III) clorua, nhôm clorua.
B) FeSO4; Fe2(SO4)3 và MgSO4.
C) K2CO3, MgSO4, Al2(SO4)3, FeSO4 và Fe2(SO4)3 là các hợp chất có trong danh sách.
Sử dụng chỉ dung dịch H2SO4 để phân biệt các chất sau:
A) Sodium chloride, sodium sulfide, sodium sulfite, sodium carbonate.
Ba, BaO, Al, và Al2O3.
C) Magnesium, Zinc, Iron, Barium.
Sử dụng duy nhất một loại kim loại để phân định các dung dịch sau: Natri sulfat, Natri cacbonat, axit clohidric và Bari nitrat.
Bằng việc bổ sung thêm nước, bạn có thể phân biệt giữa các chất sau: Natri, Magie Clorua, Sắt(II) Clorua, Sắt(III) Clorua và Nhôm Clorua.
Bằng phương pháp đun nóng và phản ứng hóa học, chúng ta có thể phân biệt được các chất lỏng sau đây: natri hidrosunfat, kali bicarbonat, magie bicarbonat, natri sulfite, bari bicarbonat.
Giải thích cách phân biệt các chất C2H4, C2H2, C2H6, CO2, SO2 bằng 2 loại thuốc thử.
Dạng số 3: Phát hiện mà không cần thử nghiệm bất kỳ loại thuốc nào khác.
Trường hợp này cần phải sử dụng để phản ứng với các lọ khác.
Người sử dụng bảng phản ứng để dễ dàng so sánh. Khi đó, các sự kiện phản ứng khác nhau sẽ phù hợp với mỗi chai. Điều này là cơ sở để phân biệt từng chai.
Phần 1: Xin vui lòng phân biệt các ống nghiệm không được đánh dấu chứa các hỗn hợp dung dịch mà không sử dụng bất kỳ phương pháp thử nghiệm nào khác.
B) Các chất Na2CO3, HCl và BaCl2. A) Muối soda, axit clohidric và muối BaCl2. B) Những chất Na2CO3, HCl và BaCl2.
B) Magie clorua, Barium clorua, axit sunfuric và kali cacbonat.
C) Na2SO4, MgSO4, CuSO4, và Ba(OH)2.
D) Muối NaCl, axit H2SO4, muối CuSO4, muối BaCl2 và kiềm NaOH.
E) Natri hydroxit, Sắt (II) clorua, Axit clohidric, Natri clorua.
F) Canxi clorua, axit clohidric, natri cacbonat, và amoni cacbonat.
G) HCl, NaCl, Ba(OH)2, Ba(HCO3)2 và Na2CO3.
H) Cu(NO3)2, Ba(OH)2, HCl, AlCl3 và H2SO4.
N) Acid clohidric, Natri hydroxit, Natri cacbonat, Magie clohidrat.
M) HCl , H2SO4 , Na2SO4 và BaCl2.
Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất.
Để xem hồ sơ đầy đủ và chi tiết, vui lòng nhấp vào nút tải xuống.
Tải về – Chủ đề phân biệt các hợp chất.: TẢI VỀ
Other articles:
Bài kiểm tra Học sinh giỏi môn Hóa lớp 12 tại tỉnh Vĩnh Phúc trong năm học 2017-2018.
Bộ sưu tập 100 bài kiểm tra Học sinh giỏi môn Hóa trung học cơ sở.
Bài kiểm tra Học sinh giỏi môn Hóa lớp 9 được tổ chức tại Gia Lộc – Hải Dương.
Chủ đề phân biệt các hợp chất.
Liên hệ qua Facebook với tài khoản Sinhh Quách.
Fanpage: PageHoahocthcs.
♥Cảm ơn bạn đã xem: Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất., Chủ đề phân biệt các hợp chất.





